|
||
ISOMERÍA EN COMPUESTOS DE COORDINACIÓN |
||
La isomería en compuestos de coordinación es parecida a la que se manifiesta en compuestos orgánicos. Por una parte diferenciamos entre isómeros estructurales y estereoisómeros. Los isómeros estructurales se diferencian en el orden en que los átomos están situados en la molécula (topología). Los estereoisómeros, sin embargo, tienen los átomos en el mismo orden pero se diferencian en la disposición espacial que ocupan. Asimismo, los estereoisómeros pueden ser confórmeros, isómeros geométricos e isómeros ópticos.Hasta aquí los parecidos, todo lo demás es diferente, empezando por los tipos de isomería estructural y de estereoisomería.
|
INDICE
|
|
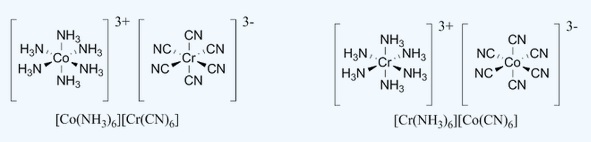
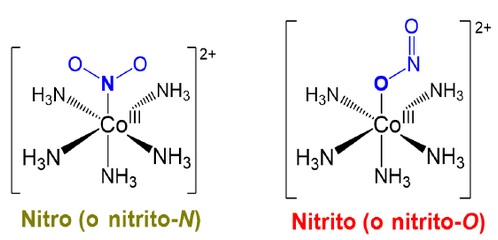
ISÓMEROS ESTRUCTURALESIsómeros que contienen el mismo número de átomos de cada clase pero unidos en un orden diferente. En los complejos de coordinación este tipo de isomería se manifiesta en el hecho de que los ligandos están unidos de manera fiferente al ion metálico central. Hay tres tipos de estos isómeros: IONIZACIÓN, COORDINACIÓN Y ENLACE.ISÓMEROS DE IONIZACIÓNEn los isómeros de ionización hay al menos dos iones que pueden actuar como ligandos. Entre ellos difieren en cual de ellos actúa como ligando o como contraion. |
||
ESTEREOISOMERÍAISOMERÍA ÓPTICA (ENANTIÓMEROS)En los compuestos de coordinación, la actividad óptica (quiralidad) surge de dos fenómenos:1.- La quiralidad inherente a un grupo orgánicoEs el caso de las aminas, en el que interconversión en torno al N (racemización) se elimina cuando se establece una unión entre el N y un metal de un compuesto de coordinación.
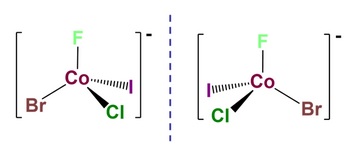
2.- La quiralidad que surge de la asimetría en torno a un centro metálicoEn este caso se pueden dar dos situaciones muy importantes:a) Quiralidad en torno a un centro metálico tetraédrico rodeado de cuatro ligandos diferentes |
||
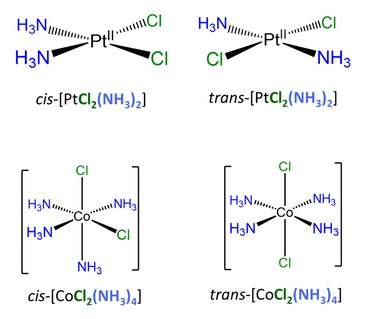
ESTEREOISOMERÍA(DIASTEREÓMEROS)En este apartado distinguiremos dos tipos de diastereómeros, los que se producen por isomería geométrica y los que surgen de la isomería conformacional (λ y δ).ISOMERÍA GEOMÉTRICAEn el caso de los complejos metálicos hay que distinguir dos tipos de isomería geométrica: la isomería cis-trans y la isomería fac-mer.En los complejos metálicos con geometría plana cuadrada u octaédrica se produce la isomería cis-trans. Isómeros geométricos cis-trans son complejos metálicos en los que dos ligandos son adyacentes unos a otros (cis) o son opuestos unos a otros (trans) en la esfera de coordinación del metal. Tanto
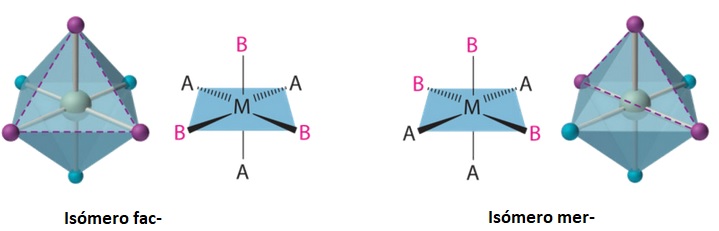
Por su parte la isomería geométrica fac-mer tiene que ver son la orientación espacial de tres ligandos en un complejo metálico de geometría octaédrica (no se produce en complejos de geometría plana cuadrada).
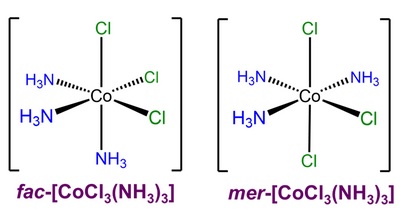
Los complejos octaédricos con tres ligandos iguales solo pueden existir en un ordenamiento fac- (de facial) o mer- (de meriodinal). En el isómero fac- los tres ligandos iguales ocupan caras triangulares opuestas del octaedro. En el isómero mer- los tres ligandos de cada clase ocupan lo que podría denominarse meridiano del octaedro.
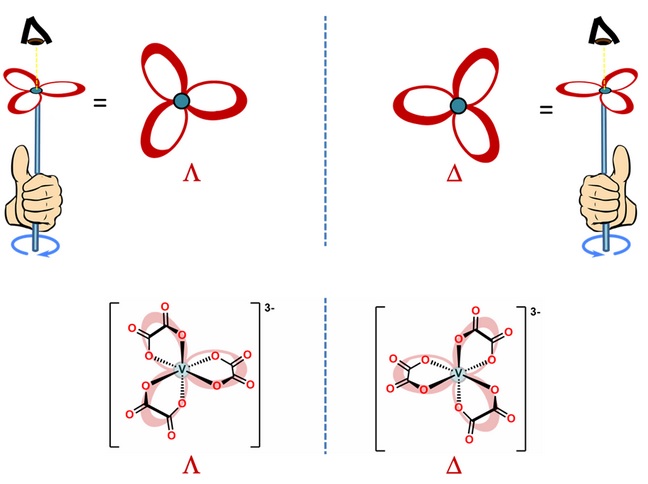
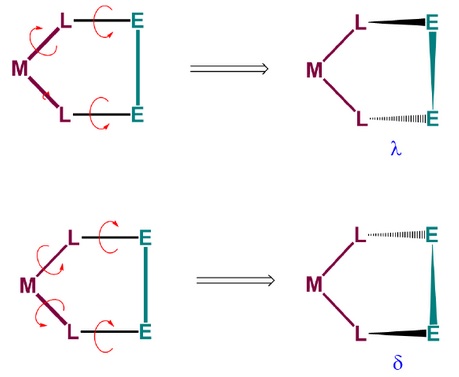
ISOMERÍA CONFORMACIONAL λ y δLos quelatos pueden formar anillos. Los de cinco miembros son especialmente estables. La isomería λ y δ está relacionada con las diferencias de estabilidad en las conformaciones de anillos de quelatos de cinco miembros que no son planos.
El proceso de formación de los confórmeros sería el siguiente (ring twist):
La asignación λ y δ se hace de la siguiente manera:
|