|
 |
|||||||||||
EL MOL |
||||||||||||
El conocimiento de las masas atómicas y moleculares permitió contar el número de átomos y moléculas que contenían las sustancias que manejábamos en el laboratorio. Esto posibilitó el nacimiento del cálculo químico (estequiometría). En el centro de este desarrollo estaba un nuevo concepto introducido por los químicos a comienzos del siglo XIX: el mol.
|
INDICE- Principios de la Teoría Atómica - Elemento (versión Dalton), compuesto, molécula y red cristalina -Explicación de las leyes ponderales -Medida de las masas atómicas (Dalton) -Medida exacta de las masas atómicas -Mol. Masa Molar -Isótopos. Unidad de masa atómica - Masa atómica relativa y absoluta - El tamaño de los átomos y las moléculas - Cálculos basados en la teoría atómica
|
|||||||||||
CONTAR NÚMERO DE ÁTOMOSImagine que un químico tiene que realizar una experiencia en la que necesita utilizar el mismo número de átomos de hidrógeno que de oxígeno, ¿qué puede hacer? ¿cómo puede contar partículas tan pequeñas?¿cómo puede estar seguro de que ha cogido el mismo número de átomos de ambos elementos?LA SOLUCIÓN ES BIEN SENCILLA:SIEMPRE COGERÁ UNA MASA DE OXÍGENO QUE SEA 16 VECES MAYOR QUE LA MASA DE HIDRÓGENO. POR EJEMPLO:1 mg de H y 16 mg de O1g de H y 16 g de O1kg de H y 16 kg de O¿Cuál ha sido el razonamiento que ha hecho?
En esas dos cantidades de hidrógeno y oxígeno hay el mismo número de átomos. No sabemos qué número es, pero eso ahora no es relevante. Lo importante aquí es que hemos podido contar números de átomos por comparación de masas. |
||||||||||||
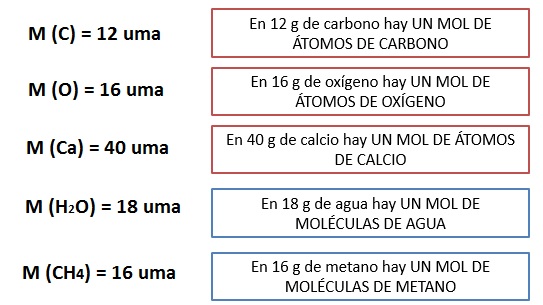
MOLDEFINICIÓN 1Mol es la cantidad de una sustancia pura (elemento o compuesto) que tiene el mismo número de partículas (átomos, iones, moléculas, ...) que átomos hay en 1 gramo de hidrógeno.
1 mol de átomos de carbono tiene una masa de 12 g1 mol de átomos de oxígeno tiene una masa de 16 g1 mol de átomos de calcio tienen una masa de 40 g1 mol de agua de moléculas de agua tiene una masa de 18 g1 mol de moléculas de metano tiene una masa de 16 g1 mol de unidades fórmula de cloruro de sodio tiene una masa de 58,5 gTodas estas cantidades de materia tienen algo en común : el número de partículas.¿Qué masa tendría 1 mol de dioxígeno O2? |
||||||||||||
MOLDEFINICIÓN 2Mol es la cantidad de sustancia pura (elemento o compuesto) que tiene una masa, expresada en gramos, igual a la masa atómica (si está formada por átomos) o masa molecular (si está formada por moléculas) o masa-fórmula (si está formada por cristales iónicos)
|
||||||||||||
MOLDEFINICIÓN 3Como es de suponer , desde que se planteó el problema del número de partículas que contiene un mol, los químicos lo buscaron utilizando diferentes técnicas analíticas.
Desde que en 1884, William Thomson hiciera la primera medida del número de partículas de un mol, los investigadores han refinado su valor. El valor actualmente aceptado es 602213670000000000000000 partículas/mol. A este número se conoce como NÚMERO DE AVOGADRO, NA.Mol es la cantidad de sustancia que contiene un número de partículas igual al número de Avogadro.El número de Avogadro es tan grande que es muy difícil de imaginar. Por ello vamos a hacer uso de un símil
|
||||||||||||
MASA MOLARLa masa molar de una sustancia es la masa de un mol de sus partículas.La masa molar de cualquier sustancia es su masa atómica, masa molecular o masa-fórmula expresada en gramos/mol
|
||||||||||||
El concepto de mol es muy importante para los químicos porque conecta el mundo macroscópico del laboratorio (masas) con el mundo microscópico de los átomos y las moléculas que no podemos ver.
Si partimos de masas, calcularemos el número de moles y, a continuación, el número de partículas. En el primer cálculo se usará la masa molar y en el segundo el número de Avogadro.
Si partimos del número de partículas, calcularemos el número de moles y, a continuación, la masa. En el primer cálculo se usará el número de Avogadro y en el segundo la masa molar
|