ADICIÓN DE AGUA A ALDEHIDOS Y CETONAS
En una disolución acuosa, un aldehido o una cetona están en equilibrio con su forma hidratada, un diol geminal (hidrato).
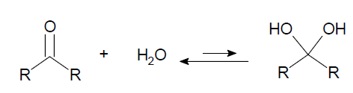
La adición está catalizada tanto por un medio ácido como básico
La adición de agua es altamente regioselectiva: el proceso siempre termina con la adición de oxígeno al carbono carbonílico
La conversión final en el equilibrio depende en gran manera de la naturaleza de los grupos unidos al carbono carbonílico.
Mecanismo de la adición de agua en medio ácido
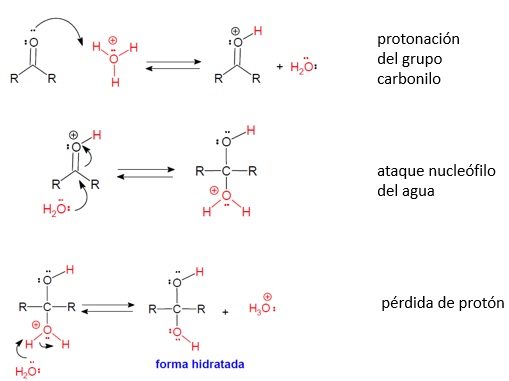
El mecanismo es similar al de la hidratación de alquenos: protonación, adición, desprotonación
Mecanismo de la adición de agua en medio básico
En medio básico el mecanismo es diferente. En este caso el ataque nucleofílico lo produce el ion hidroxilo (no la molécula de agua como en medio ácido) y el proceso tiene dos etapas: 1) adición de OH- al carbono carbonílico y 2) protonación del oxígeno carbonílico. En este caso no es necesaria activación inicial del carbono carbonílico ya que el ion hidroxilo es un nucleófilo más fuerte que la molécula de agua.
