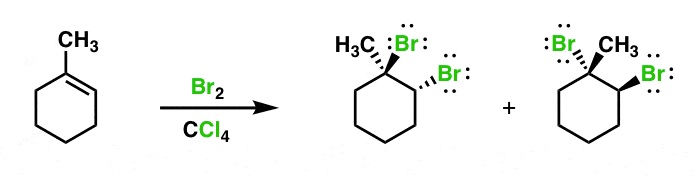
ADICIÓN DE HALÓGENOS
ADICIÓN DE HALÓGENOS A ALQUENOS


Los halógenos pueden actuar como electrófilos ¿Cómo lo consiguen?
A medida que la molécula de halógeno se aproxima, por ejemplo, al doble enlace C=C, los electrones del doble enlace repelen a los de la molécula de halógeno provocando una polarización del enlace que une sus átomos. Esto crea un momento dipolar en la molécula de halógeno. Esta situación permite que el enlace entre los átomos de halógeno se rompa heterolíticamente, permitiendo que uno de ellos adquiera carga positiva y quede unido a uno de los carbonos del doble enlace. El otro átomo del halógeno adquiere carga negativa y puede actuar como nucleófilo en otra etapa del proceso.

La adición de halógenos a alquenos no es regioselectiva porque los dos átomos que se unen al doble enlace son iguales pero si es estereoselectiva ANTI. Los átomos de halógeno quedan orientados hacia los lados contrarios de la molécula de alqueno dando como producto un dihaluro vecinal. Esta sustancia, en el caso de poseer un estereocentro, será una mezcla racémica ya que el ataque por las dos caras del alqueno tiene la misma probabilidad de ocurrir.

En las halogenaciones de alquenos se suelen utilizar bromo o cloro. La reacción con iodo es demasiado lenta y con flúor puede llegar a ser explosiva.
En estas reacciones se utilizan disolventes inertes como diclorometano o tetracloruro de carbono, cuyo papel es únicamente disolver los reactivos. En el caso de utilizar disolventes polares próticos como agua o alcoholes, el proceso se complica porque el disolvente participa en la reacción produciendo halohidrinas.
Mecanismo
En la primera etapa (lenta) el alqueno ataca al electrófilo, que en este caso es la molécula de Br2. Como consecuencia del ataque, los electrones del enlace pi forman un nuevo enlace sigma entre un C y el Br, quedando el otro átomo de Br con el par de electrones de enlace (ion bromuro). Sin embargo, este proceso no forma un carbocatión ya que un par de electrones del Br recien unido al C forma un nuevo enlace con el otro átomo de C del (antiguo) doble enlace (que momentáneamente ha quedado con déficit electrónico). Como resultado, en lugar de un carbocatión, se forma un ion bromonio cíclico (en general, halogenonio).

En resumen, al formar el primer enlace C-Br el átomo de bromo actúa como electrófilo y, seguidamente, al formar el segundo, como nucleófilo.

Este intermedio cíclico es un anillo de tres miembros inestable a causa de la tensión de enlace y la carga positiva alojada en el átomo de bromo. Por ello, es susceptible de un ataque nucleófilo.

En la segunda etapa, el ion bromonio sufre un ataque nucleofílico por parte del ion bromuro formado en la primera etapa. Este ataque SN2 rompe la unión C-Br, elimina la tensión de enlace y forma el producto final.

Aunque este dihaluro puede ser quiral, el producto obtenido no es ópticamente activo ya que es una mezcla racémica. La adición inicial de bromo al doble enlace ocurre con la misma probabilidad por ambas caras del alqueno formando dos iones bromonio y, posteriormente, una pareja de enantiómeros en la misma proporción.
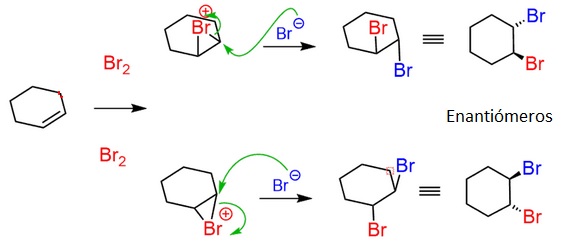
EJERCICIO
Determinar el o los productos principales en el siguiente proceso de adición de bromo.

ADICIÓN DE HALÓGENOS A ALQUINOS
La adición de halógenos a alquinos tiene lugar de manera similar a la que se ha descrito en el caso de los alquenos.
Si se agrega 1 equivalente de halógeno se obtiene un trans diahaloalqueno.

El mecanismo es el siguiente:

En una primera etapa se forma el ion bromonio de tres centros. A continuación, en la segunda etapa, el ion bromuro ataca al ion bromonio provocando la apertura del anillo y la formación de un nuevo enlace sigma C-Br.
Si la reacción tiene lugar con exceso de bromo se forma un derivado tetrahalogenado.