FACTORES QUE INFLUYEN EN LA ACIDEZ
PRÍNCIPIO GENERAL: Cuanto más estable sea el ión formado por el ácido al desprenderse del protón, mayor será su fuerza ácida

Por tanto, todos los factores que aumenten la estabilidad de la base conjugada, aumentarán la fuerza ácida de una especie química
CARGA DEL ÁTOMO QUE HA DE DESPRENDERSE DEL PROTÓN
¿Qué especie es más ácida el agua o el ion hidronio? ¿el amoniaco o el ion amonio?

En el agua el átomo central de oxígeno no tiene carga formal. En el ion hidronio tiene una carga formal positiva. Si ambas especies deben perder un ion H+, es esperable que el proceso sea más sencillo en el ion hidronio que en el agua. Cuando más positiva sea la carga del átomo unido al hidrógeno ionizable, mayor será la fuerza ácida.
Un razonamiento similar podemos hacer en el caso del amoniaco y el ion amonio. Este último, con un nitrógeno cargado positivamente, debe ser más ácido que el primero.
ELECTRONEGATIVIDAD DEL ÁTOMO QUE PORTA LA CARGA NEGATIVA
Permite comparar átomos del mismo periodo de la Tabla Periódica
La pérdida del ion H+ suele venir acompañada con la formación de una carga negativa sobre un heteroátomo.
Cuanto más electronegativo sea el átomo que porta la carga negativa más estable será el ión formado y, por tanto, más ácida será la especie química original.
El agua será más ácida que el amoniaco por que el ion hidroxilo es más estable que el ión amiduro, ya que el oxígeno (al ser más electronegativo) porta mejor la carga negativa que el nitrógeno. La misma comparación podríamos hacer entre el amoniaco y el metano.
En el caso de que queramos comparar átomos de distintos periodos del SP hay que tener en cuenta otros factores.
TAMAÑO DEL ÁTOMO QUE PORTA LA CARGA NEGATIVA
Permite comparar átomos del mismo grupo de la Tabla Periódica
Orden de acidez: HI > HBr > HCl > HF
¿Qué ocurre cuando la carga negativa es soportada por átomos de un mismo grupo del SP?
En este caso debemos fijarnos en el tamaño del ión, más que en su electronegatividad. El ácido HI es más fuerte que el HF, porque el ión ioduro es mucho más voluminoso que el ión fluoruro, alojando mejor la carga negativa (a pesar de que el átomo de fluor es más electronegativo que el átomo de iodo)

¿Cuál es más fuerte como ácido, un tiol o un alcohol?

Si ambos perdieran un protón darían lugar a sendos iones con carga negativa: ¿Qué átomo S o O alojará mejor la carga negativa?. Fíjese que S y O pertenecen al mismo grupo del SP.
RESONANCIA
¿Por qué el fenol es un ácido más fuerte que el etanol?

La presencia de una carga negativa sobre un átomo es una fuente de inestabilidad. Cuanto más repartida esté esa carga más estable será el anión. La resonancia permite, en algunos caso, deslocalizar la carga negativa de las bases conjugadas.
El fenol tiene un acentuado carácter ácido gracias a la estabilización por resonancia del ión fenolato. Este hecho no se produce en el ión etóxido (no tiene formas resonantes y la carga negativa está concentrada en el átomo de oxígeno). Por ello el fenol es notablemente más ácido que el etanol, a pesar de ser los dos alcoholes.
¿Por qué el ácido acético es un ácido más fuerte que el fenol?
Más importante que el número de formas resonantes es la estabilidad de éstas. En el ion acetato hay solo dos formas resonantes y en el ion del fenol hay cuatro, sin embargo, el ácido acético es un ácido más fuerte que el fenol. En el caso del ion acetato, las cargas negativas están situadas en átomos de oxígeno, más electronegativos que los de carbono. En el caso del ion fenóxido, tres de las formas resonantes tienen carga negativa sobre átomos de carbono y, además, esas formas resonantes no son aromáticas.
La presencia de grupos dadores o aceptores de carga unidos al anillo bencénico provocará que el ion formado sea más o menos estable. ¿Qué sustancia es más ácida, el fenol, el p-nitrofenol o el p-metilfenol?. Recuerde que el grupo nitro es aceptor de carga y el grupo metilo es dador de carga.
Una ayuda: el ácido pícrico (trinitrofenol) es extremadamente fuerte, su pKa=0,25

Compare la acidez de los H indicados en cada molécula. Señale el que considere que es más ácido en cada caso.

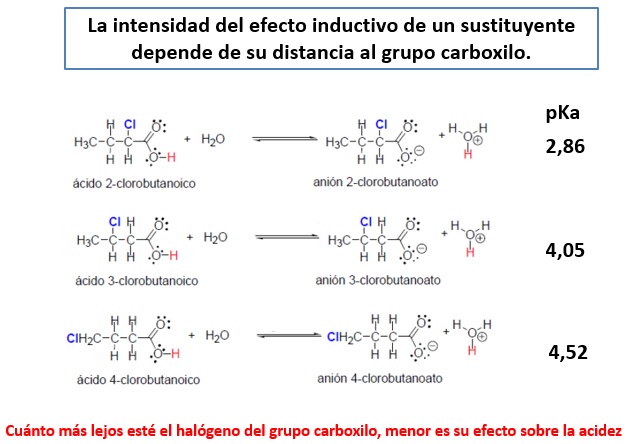
EFECTO INDUCTIVO
El efecto inductivo electrón atrayente (-I) aumenta la acidez

La presencia de un átomo o grupo de átomos que atraigan carga eléctrica por efecto inductivo contribuirá a disminuir la concentración de carga eléctrica en el heteroátomo de la base conjugada. Eso aumentará su estabilidad y, por tanto, la acidez de la especie original.
El ácido cloroacético es mucho más fuerte que el ácido acético, porque el ion cloroacetato es más estable que el ión acetato.
El efecto inductivo electrón dador (+I) disminuye la acidez

Sin embargo, si por efecto inductivo, el grupo cede carga eléctrica al átomo que ya porta la carga negativa en la base conjugada, se contribuirá a inestabilizarla y, por tanto, a disminuir la acidez de la especie original.
El metanol es un ácido más fuerte que el etanol porque el ion metóxido es más estable que el etóxido. Este último estaría inestabilizado por la cesión de carga que provoca el grupo metilo.


TIPO DE ORBITAL QUE ALOJA LA CARGA
Cuanto mayor sea el carácter s de un orbital híbrido mejor alojará los electrones. Ello se debe a que cuanto mayor sea el carácter s de un orbital, su densidad electrónica está más próxima al núcleo.


EJEMPLO
COMPARACIÓN DE LOS FACTORES
¿Cuál es el átomo de H más ácido de entre los resaltados?





