MECANISMOS DE REACCIÓN
El mecanismo de una reacción es el detalle de las transformaciones graduales que sufren las moléculas de las sustancias reaccionantes hasta convertirse en productos de la reacción.
El mecanismo debe explicar los siguientes hechos:
- Debilitamiento de los enlaces entre átomos de los reactantes
- Formación de un complejo activado inestable
- Aparición de nuevos enlaces entre los átomos que forman los productos
- Variación de la energía del proceso

Como en el paso controlante de la velocidad participan los dos reactivos, la velocidad de reacción dependerá de las concentraciones de ambos, es decir, su ecuación cinética será de segundo orden.
Esta es una reacción concertada, ya que en un solo paso se rompe el enlace C-X y se forma el enlace C-O. Ambos procesos tienen lugar cuando se ha formado una especie de alta energía denominada complejo activado.

En el máximo de la curva de energía potencial se encuentra el complejo activado. La energía de activación es la diferencia entre los niveles energéticos de los reactivos y el complejo activado.


Paso 1 (lento).- El enlace C-Cl se rompe heterolíticamente. El átomo de cloro se lleva el par de electrones, dando lugar a un carbocatión terciario
Paso 2 (rápido).- El carbocatión sufre un ataque por parte del nucleófilo OH-- dando lugar al alcohol
Como en el paso controlante de la velocidad (etapa lenta) solo participa uno de los reactivos (el haluro), la velocidad de reacción solo dependerá de su concentración, es decir, su ecuación cinética será de primer orden.

Esta es una reacción NO concertada, ya que los enlaces se rompen y se forman en etapas diferentes. En ambas etapas se formarán sendos complejos activados.

En el diagrama de energía potencial se observa la presencia de dos máximos de energía que corresponden a los complejos activados de cada una de las etapas del proceso. Entre ellos hay un mínimo de energía que corresponde a la formación de un intermedio de reacción, el carbocatión. El intermedio de reacción es producto del primer paso pero es el reactivo del segundo, por tanto, es una especie química que se forma y consume a lo largo de la reacción, no aparece entre los productos.
Como la energía de activación del primer paso es mayor que la del segundo, la velocidad del primer paso es menor que la del segundo. Esto quiere decir que el paso controlante de la velocidad (lento) es el primero.

POSTULADO DE HAMMOND

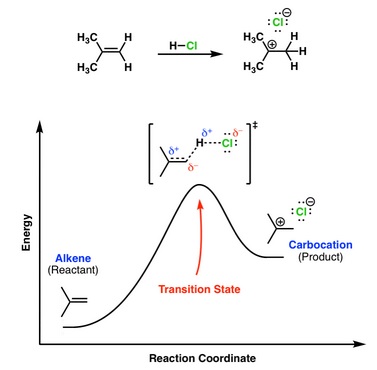
En una reacción exotérmica, el estado de transición (complejo activado) está más próximo en energía y estructura a los reactivos que a los productos. En una reacción endotérmica, el estado de transición está más próximo en energía y estructura a los productos.
Por ejemplo, en la reacción endotérmica entre un alqueno y un ácido para formar un carbocatión, el estado de transición debe parecerse más al carbocatión que al alqueno.
FLECHAS CURVAS (Curly arrows)
Es práctica habitual que los movimientos electrónicos que tienen lugar durante la reacción se indiquen con flechas curvas (curly arrows). En general se usan dos tipos de flechas:
Una flecha con la cabeza completa que indica el desplazamiento de un par de electrones
Una flecha con media cabeza que indica el desplazamiento de un electrón
![]()
EJEMPLO
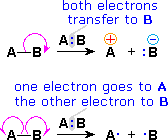
ROTURA DE ENLACES
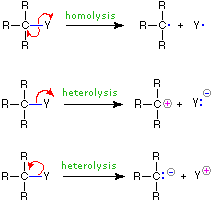
FORMACIÓN DE ENLACES

Otras flechas usadas en la representación de los mecanismos de reacción
Flecha de reacción![]()
Flecha de equilibrio![]()
Flecha de resonancia![]()

WEB CON TUTORIALES SOBRE MECANISMOS DE REACCIÓN
U.CAN Understand Curved Arrow Notation
En esta web de University of South Dakota se pueden ver paso a paso los mecanismos de algunas reacciones orgánicas de interés en flash:
Bromación
del propano mediante radicales libres
Hidrobromación
electrofílica del propeno
Hidrobromación
por radicales libres del propeno
Bromación
electrofílica del cis-2-buteno
Transposición
de carbocationes
SN2
Sustitución nucleofílica de segundo orden
SN1
Sustitución nucleofílica de primer orden
E1
Eliminación de primer orden
E2
Eliminación de segundo orden
Formación
de epóxidos
Ruptura
ácida de epóxidos
Ruptura
alcalina de epóxidos
Reacción
de Diels-Alder
Bromación
electrofílica del benceno
Síntesis
de cianohidrinas
Esterificación
de Fischer
Hidrólisis
alcalina del acetato de etilo
Transposición
de Beckman
Organic Reaction Mechanisms
ChemTube 3D
INTERACTIVE ORGANIC MECHANISMS
Tutorial interactivo de Oxford University. Necesita Flash Player
Su objetivo es ayudar a los estudiantes a representar el mecanismo de reacción mediante flechas que indiquen el movimiento de electrones y especies químicas a lo largo de la reacción.
Sustitución Nucleofílica
SN1 Reacciones
SN2 Reacciones
Eliminación
E1 Reacciones
E2 Reacciones

