ESPECTROSCOPÍA RMN
INTERPRETACIÓN ESPECTRO RMN
Para interpretar el espectro RMN hay que tener en cuenta los siguientes aspectos:
1.- Desplazamiento químico
2.- Línea integral
3.- Acoplamiento spin-spin
ESPECTROSCOPÍA: ORIGEN DEL PROBLEMA
ESPECTROSCOPÍA ULTRAVIOLETA-VISIBLE
ESPECTROS IR DE SUSTANCIAS ORGÁNICAS
Desplazamiento químico
Indica el tipo de protón que provoca cada señal
En un espectro H-RMN habrá tantas señales como átomos de hidrógeno diferentes haya en la especie química. Hablamos de equivalencia química para referirnos a protones que cumplen el mismo rol y, por tanto, son equivalentes de cara al análisis RMN.
Lo mismo ocurre en un espectro C13-RMN.
Equivalencia Química
Normalmente se emplean tres métodos para identificar el número de tipos de hidrógeno en una molécula:
1.- Método de sustitución
Se sustituye cada hidrógeno por un átomo diferente (por ejemplo Cl) y se comprueba si se obtienen compuestos diferentes. Por ejemplo, en el cloroetano hay dos tipos de hidrógeno porque sustituyendo por cloro se pueden obtener dos compuestos diferentes, el 1,1-dicloroetano y el 1,2-dicloroetano
2.- Descripción verbal
Si necesita emplear distintos términos para describir dos átomos de hidrógeno es que representan dos tipos diferentes. Por ejemplo un -OH es diferente a un -CH , un -CH3 es diferente a un -CH2- y un sp3 C-H es diferente a un sp C-H
3.- Simetría
Los átomos de carbono que puedan ser intercambiados por operaciones de simetría son equivalentes
¿Cuántos hidrógenos diferentes hay en las siguientes moléculas?¿Y átomos de carbono?
En la acetona hay un tipo de átomos de hidrógeno y dos tipos de átomos de carbono
¿los reconoce?

RMN H un pico a: 2,16 ppm

RMN C dos picos a: 206 y 31 ppm
En el pentano hay 3 tipos de átomos de hidrógeno y tres tipos de átomos de carbono
¿los reconoce?

RMN H tres picos a: 1,30; 1,26 y 0,88 ppm

RMN C tres picos a: 34, 22 y 14 ppm
En el fenol hay 4 tipos de átomos de hidrógeno y cuatro tipos de átomos de carbono
¿los reconoce?
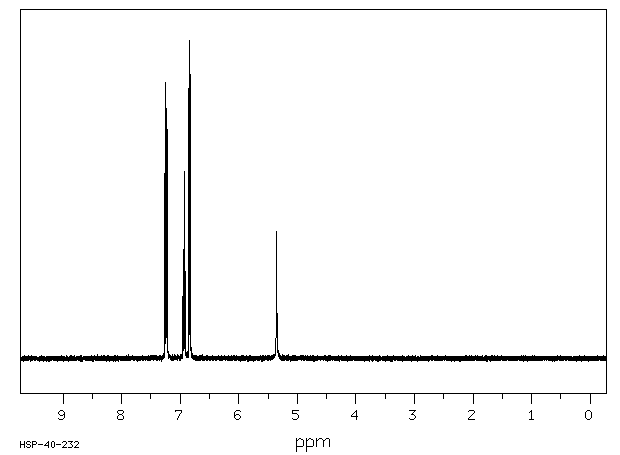
RMN H cuatro picos a: 7,24; 6,93; 6,84 y 5,35 ppm

RMN C cuatro picos: 155; 130, 121 y 115 ppm
Homotópicos: átomos o grupos cuya sustitución da lugar al mismo producto
Por ejemplo son homotópicos los H del bromo metano, su sustitución por Cl siempre daría el mismo producto: bromoclorometano
Enantiotópicos: átomos o grupos cuya sustitución da lugar a dos enantiómeros
Los H del carbono 1 del bromoetano son enantiotópicos porque la sustitución de uno de ellos da lugar a un enantiómero diferente
Diastereotópicos: átomos o grupos cuya sustitución da lugar a dos diastereómeros
Los H del carbono 1 del 1-bromo-1-cloroetano son diastereotópicos porque la sustitución de uno de ellos da lugar a dos diatereómeros
Línea integral
La línea integral (verde) indica la intensidad del pico e informa del número de protones que producen la señal
En el primer caso las dos señales están en la proporción 3:2. Como el número total de protones es de 10, una corresponde a 6 protones y la otra a 4
En el segundo caso las señales están en la proporción 3:1. Como el número total de protones es 8, una corresponde a 6 protones y la otra a 2
En el tercer caso las señales están en la proporción 1:1. Como el número total de protones es 6, cada una corresponde 3 protones
A continuación se muestra el espectro RMN del etanol. La línea integral tiene saltos que corresponden a 1, 2 y 3 átomos de hidrógeno.

Acoplamiento spin-spin (conectividad de núcleos)
Hasta ahora hemos mostrado espectros RMN que tenía señales que eran picos independientes, sin embargo, la realidad es que en muchos casos los picos aparecen como grupos de picos debido al acoplamiento que sufren los espines con núcleos vecinos.
El acoplamiento espín-espín informa de cómo están conectados los protones
El espectro RMN del 1,1-dicloroetano presenta dos señales:
δ = 5,9 ppm ; integración = 1 corresponde a -CHCl2
δ = 2,1 ppm ; integración = 3 corresponde a -CH3
El desdoblamiento de las señales se produce por el efecto del campo magnético vecino sobre el aplicado externamente, provocando que la frecuencia de resonancia cambie.
Efecto de grupo -CH- sobre el grupo -CH3
El espín del grupo metino -CH puede adoptar dos orientaciones con respecto al campo externo aplicado. Como resultado de ello la señal del grupo -CH3 vecino se desdobla en dos líneas de igual intensidad, un doblete.
Efecto del grupo -CH3 sobre el grupo -CH
Los espines de los tres protones del grupo metilo pueden adoptar 8 combinaciones, que se pueden agrupar en cuatro opciones diferentes (en dos casos hay tres combinaciones equivalentes). Como resultado de ello la señal del grupo vecino -CH se desdobla en cuatro líneas con intensidades respectivas 1:3:3:1, un cuartete.
Generalizando este análisis podemos afirmar que la proximidad de n protones equivalentes en un carbono vecino provoca el desdoblamiento de la señal en n+1 líneas, el número de éstas se conoce como multiplicidad de la señal. Los protones equivalentes no se acoplan entre sí. Si los protones vecinos no son equivalentes el acoplamiento es más complejo.
Cuando en el acoplamiento intervienen dobles enlaces la situación no sigue la regla del n+1
Constante de acoplamiento J
La constante de acoplamiento mide la intensidad de la interacción entre pares de protones
En un sistema del tipo, Ha-C-C-Hb la constante de acoplamiento de Ha con Hb, Jab, debe ser igual a la del acoplamiento de Hb con Ha, Jba, por tanto Jab = Jba.
La intensidad de las líneas en los acoplamientos de señales viene dada por el triángulo de Pascal












