GASES
PROPIEDADES
- Características de la materia en estado gaseoso. Teoría cinética de los gases
-Leyes de Charles y Gay-Lussac
- Ley de las presiones parciales de Dalton
- Teoría cinética de los gases
Las principales características de la materia en estado gaseoso son las siguientes:
1.- Los gases ocupan completamente el volumen del recipiente que los contiene. No tienen forma propia.

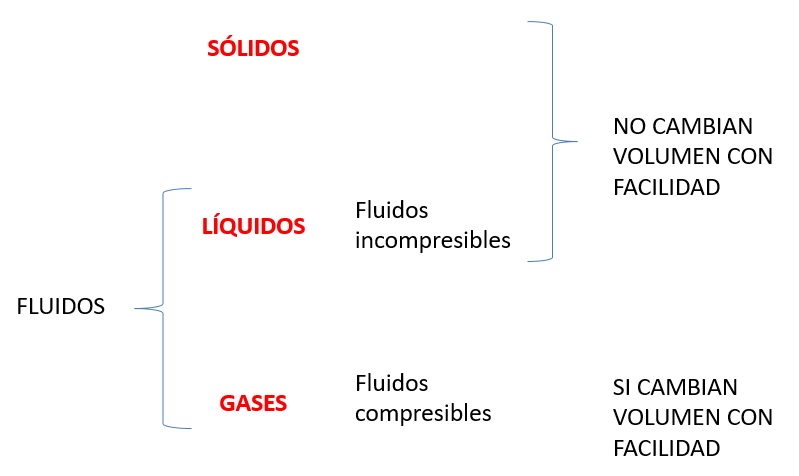
2.- El volumen de los gases cambia con facilidad cuando se modifican la presión o la temperatura. Eso no ocurre ni en los sólidos ni en los líquidos.

Los gases y los líquidos son conocidos como fluidos, pueden fluir (como ocurre con la pasta de dientes). Sin embargo, hay grandes diferencias entre gases y líquidos.
Los líquidos son incompresibles porque sus partículas están muy próximas. Si ejercemos presión sobre un líquido será muy difícil que logremos aproximar más sus moléculas. Eso no ocurre con los gases, en ellos las partículas están muy separadas y si ejercemos presión podemos aproximarlas (hay que recordar que entre las partículas de los gases hay vacio).

La teoría cinética de los gases, propuesta por Bernouilli (siglo XVIII) y posteriormente desarrollada por Clausius y Boltzmann (siglo XIX) explica las propiedades de los gases haciendo uso de un pequeño número de postulados:
1.- LOS GASES ESTÁN CONSTITUIDOS POR PARTÍCULAS QUE SE MUEVEN CAÓTICAMENTE EN LÍNEA RECTA
2.- EL MOVIMIENTO DE LAS PARTÍCULAS CAMBIA CUANDO CHOCAN CON OTRAS PARTÍCULAS O LAS PAREDES DEL RECIPIENTE
3.- EL VOLUMEN DE LAS PARTÍCULAS ES DESPRECIABLE COMPARADO CON EL RECORRIDO MEDIO
4.- ENTRE LAS PARTÍCULAS NO HAY FUERZAS ATRACTIVAS NI REPULSIVAS
Puedes ampliar imformación en EDUCAPLUS
A LA VISTA DE LA TEORÍA CINÉTICA DE LOS GASES, EXPLICA LOS SIGUIENTES HECHOS:
- Cuando colocamos un globo al sol, se hincha
- Cuando está inflado, un balón de futbol está duro a pesar de que sólo contiene aire en su interior
- Las cuatro ruedas de un coche soportan el peso del auto, y sólo contienen aire
- Un globo con aire caliente se eleva
- Si colocamos un ambientador en la esquina de una habitación, al poco tiempo todo el aire en ella huele a perfume
¿Los gases tienen masa? ¿Los gases pesan? ¿Los gases ocupan volumen?
Si todavía tiene dudas acerca del carácter material de los gases y de que los gases pesan, mire estos vídeos:
Medida directa del peso del aire
El peso del aire de nuestra atmósfera provoca la presión atmosférica. Sus efectos pueden ser impresionantes
Por cierto, después de lo que ha visto no le será muy difícil explicar cómo funciona un BARÓMETRO de Torricelli
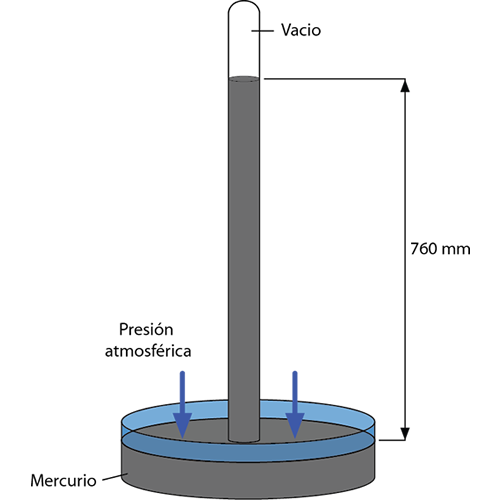
El peso del aire de nuestra atmósfera impide que el mercurio salga de la columna. Por término medio, la presión atmosférica es similar a la que ejerce una columna de 760 mm de mercurio.