
ESTRUCTURA Y PROPIEDADES
ALDEHIDOS Y CETONAS

Aldehidos y cetonas son compuestos orgánicos simples que contienen el grupo carbonilo (C=O). Son simples en el sentido de que no tienen otros grupos reactivos como OH, OR o X unidos al carbono del grupo carbonilocomo ocurre en los ácidos carboxílicos, los ésteres o los haluros de acilo.
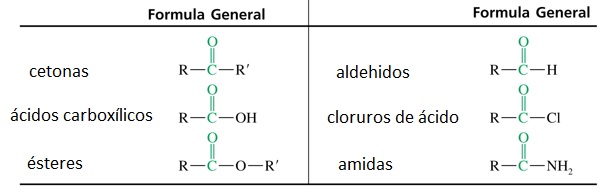
En los aldehidos, el grupo carbonilo está unido a un H y a otro H, o más frecuentemente, a un grupo alquilo o arilo. En las cetonas el grupo carbonilo está unido a dos grupos alquilo (o arilo).
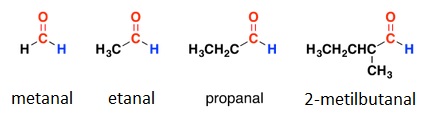

A continuación se citan productos naturales que contienen el grupo carbonilo. Unos de origen vegetal:

y otros de origen animal:

ESTRUCTURA
En el grupo carbonilo, tanto el átomo de carbono como el de oxígeno tienen hibridación sp2.
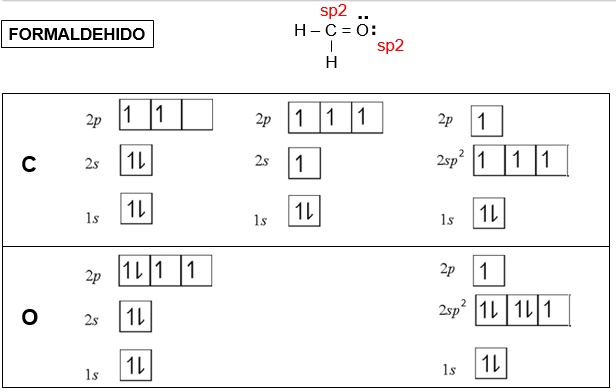
La aproximación de los dos átomos produce un enlace sigma por solapamiento frontal de dos orbitales híbridos sp2 y un enlace pi por solapamiento lateral de dos orbitales pz semillenos. En consecuencia, la estructura formada es plana con ángulo típico de 120 º.

Por otra parte, el oxígeno es un átomo bastante más electronegativo que el carbono, por tanto, tiene una marcada tendencia a atraerse hacia sí los electrones del enlace C=O. Eso le da al grupo carbonilo una alta polaridad.

Por tanto, el carbono del grupo carbonilo será un centro electrófilo atacable por nucleófilos (por ejemplo iones cianuro) y el oxígeno será un centro nucleófilo atacable por electrófilos (por ejemplo un protón). Además hay que tener en cuenta que la presencia del doble enlace C=O aumenta la acidez de los H unidos al carbono alfa. La pérdida de ese H alfa (por la acción de una base) provocaría la aparición de una carga negativa sobre el carbono alfa que puede estabilizarse por resonancia con el grupo carbonilo.

La presencia de un hidrógeno unido al grupo carbonilo en los aldehidos hace que este tipo de sustancias se oxide con facilidad hasta ácidos carboxílicos. Sin embargo, la ausencia de ese átomo de H en las cetonas, provoca que estas sustancias sean refractarias a la oxidación. Este proceso solo se consigue con oxidantes muy fuertes que rompen los enlaces C-C. Esta diferencia entre aldehidos y cetonas se utiliza para distinguirlos, por ejemplo en el ensayo de Tollens (reacción del espejo de plata).
PROPIEDADES FÍSICAS
Los aldehidos y las cetonas son sustancias polares pero no pueden formar puentes de hidrógeno por sí solas ya que, aunque disponen de pares de electrones que compartir, no disponen de átomos de H ionizables (en enlaces OH). Esto provoca que entre sus moléculas se manifiesten fuerzas de dispersión e interacciones dipolo-dipolo dando lugar a que sus puntos de ebullición sean más elevados que los de los alcanos de similar estructura (estos solo tienen fuerzas de dispersión) pero menores que los de los alcoholes de similar tamaño (estos tienen, además, puentes de hidrógeno).

Sin embargo (al igual que los éteres), los aldehidos y las cetonas pueden actuar como aceptores de hidrógeno y formar puentes de hidrógeno, por ejemplo, con el agua. Esto provoca que los miembros de estas familias de sustancias con pequeño número de átomos de carbono sean solubles en agua.

La solubilidad disminuye rápidamente con el aumento del número de átomos de carbono.
