

ENLACE COVALENTE
TEORÍA DE LEWIS Y MÉTODO DE REPULSIÓN DE PARES DE ELECTRONES DE LA CAPA DE VALENCIA
TEORÍA DE LEWIS

En 1916 Gilbert Newton Lewis propuso que el enlace covalente entre átomos se produce por compartición de pares de electrones, mecanismo por el que cada uno individualmente podría alcanzar ocho electrones en su capa de valencia
El fundamento de este principio hay que buscarlo en la denominada regla del octeto, consecuencia del desarrollo del modelo de Bohr y del descubrimiento de los gases nobles, sustancias de notable inercia química y ocho electrones en su capa de valencia.
Formación de la molécula de flúor

Por separado, cada átomo de fluor tiene 7 electrones en su corteza electrónica. Sin embargo, cuando se acercan y comparten un par de electrones, cada uno de ellos llega a tener 8 electrones en su capa de valencia. Este hecho permanecerá siempre que la molécula F2 se mantenga unida. Según Lewis, el átomo F es más estable dentro de la molécula F2 que aislado. Esto se demuestra con los diagramas de energía potencial. Por ejemplo, cuando se aproximan dos átomos de H la energía potencial del sistema pasa por un mínimo cuando los núcleos se encuentran a una cierta distancia. Puede comprobarlo con la siguiente simulación.
INDICE
- Teorías acerca del enlace químico
- Estudio energético de la formación del enlace iónico. Energía reticular
-Teoría del enlace-valencia y Hibridación
- Energía de disociación de enlace
ESTRUCTURAS DE LEWIS
Indican la distribución de electrones en la molécula (NO SU FORMA). Permiten determinar los enlaces que unen los átomos y los electrones no compartidos que contienen.
Antes de abordar la construcción de las estructuras de Lewis de las moléculas, es necesario conocer los símbolos de Lewis de los elementos químicos:
SÍMBOLO ELEMENTO + ELECTRONES EN CAPA DE VALENCIA

IMPORTANTE: Un átomo de carbono con 4 electrones en la capa de valencia es neutro. Lo mismo ocurre, por ejemplo, con un átomo de nitrógeno si tiene 5 electrones en su capa de valencia. En el caso del oxígeno serían necesarios 6 electrones.
PROCEDIMIENTO ESTÁNDAR PARA DETERMINAR ESTRUCTURAS DE LEWIS
1.- DETERMINAR EL NÚMERO DE ELECTRONES EN LAS CAPAS DE VALENCIA DE LOS ÁTOMOS QUE FORMAN LA ESPECIE QUÍMICA
2.- CONSTRUIR UNA ESTRUCTURA DE LEWIS PRELIMINAR COLOCANDO COMO ÁTOMO CENTRAL EL MENOS ELECTRONEGATIVO (NO PUEDE SER H). SE USAN PARES DE ELECTRONES PARA UNIR EL ÁTOMO CENTRAL CON LOS PERIFÉRICOS. LOS PARES DE ELECTRONES SOBRANTES SE COLOCAN SOBRE LOS ÁTOMOS PERIFÉRICOS Y, POR ÚLTIMO, SOBRE EL CENTRAL AL OBJETO DE CUMPLIR EN LA MEDIDA DE LO POSIBLE LA REGLA DEL OCTETO.
SI SE CUMPLE LA REGLA DEL OCTETO EN TODOS LOS ÁTOMOS HEMOS TERMINADO LA ESTRUCTURA DE LEWIS. EN CASO CONTRARIO, SE CONTINÚA
3.- COLOCAR ENLACES MÚLTIPLES PARA CONSEGUIR CUMPLIR LA REGLA DEL OCTETO EN TODOS LOS ÁTOMOS
4.- CALCULAR LA CARGAS FORMALES
5.- VALORAR LA EXISTENCIA DE FORMAS RESONANTES
EJEMPLO: MOLÉCULA AGUA
1.- Nºe capa valencia = 6 + 2x1 = 8 (4 pares)
2.-
3.- No es necesario. Todos los átomos cumplen la regla del octeto
4.- No hay cargas formales
5.- No hay formas resonantes
En la molécula de agua hay dos enlaces covalentes simples que conectan cada uno de los átomos de hidrógeno con el átomo central de oxígeno. El átomo de oxígeno tiene dos pares de electrones sin compartir
EJEMPLO: MOLÉCULA DE AMONIACO
1.- Necv = 5 + 3x1 = 8 (4 pares)
2.-
3.- No es necesario. Todos los átomos cumplen la regla del octeto
4.- No hay cargas formales
5.- No hay formas resonantes
En la molécula de amoniaco hay dos enlaces covalentes simples que conectan cada uno de los átomos de hidrógeno con el átomo central de nitrógeno. El átomo de nitrógeno tiene un par de electrones sin compartir.
EJEMPLO: MOLÉCULA DE OZONO
1.- Necv = 6 + 6 + 6 = 18 (9 pares)
2.-
El átomo central no cumple la regla del octeto
3.-
Ahora el átomo central sí cumple la regla del octeto
4.- Hay cargas formales. El átomo O de la izquierda no tiene carga formal [6-(4+2)]. El átomo O central tiene carga +1 [6-(2+3)]. El átomo O de la derecha tiene carga -1 [6-(6+1)].
La molécula de ozono es neutra pero en su interior hay átomos con carga

5.- Si hay formas resonantes. La molécula de ozono tiene dos formas resonantes idénticas
En la molécula de ozono hay dos enlaces covalentes, uno simple y otro doble que cambian continuamente de posición. Es como si cada uno de ellos fuera todo el tiempo un enlace intermedio entre simple y doble. Lo mismo ocurre con las cargas formales. El átomo central siempre tiene una carga formal positiva, pero los átomos de oxígeno laterales se comportan como si siempre tuvieran 1/2 de carga negativa.

Híbrido de resonancia del ozono
Las cargas formales se calculan restando a los electrones de valencia del átomo neutro (6 en el oxígeno, 5 en el nitrógeno, 4 en el carbono) el número de electrones no compartidos y la mitad de los los electrones compartidos.

H: Carga formal = 1-(0+1) = 0
C (CH3) Carga formal = 4 - (0+4) = 0
C (COO) Carga formal = 4 - (0+4) = 0
O (superior) Carga formal = 6 - (4+2) = 0
O (inferior) Carga formal = 6 - (6+1) = -1
El ion acetato tiene globalmente carga -1 porque en su interior hay un átomo de oxígeno que tiene carga -1
Determinación cargas formales Video
LAS FORMAS RESONANTES EXISTEN CUANDO LA ESPECIE QUÍMICA PUEDE SER REPRESENTADA POR MÁS DE UNA ESTRUCTURA DE LEWIS
Formas resonantes en iones
ver resonancias de especies orgánicas
En la siguiente web de la Universidad de Valencia podrá manejar estructuras de Lewis y colocar pares de electrones no compartidos
VISUALIZACIONES EN QUÍMICA
En esta página podrás convertir la fórmula de cualquier molécula orgánica en su estructura de Lewis
WOLFRAM / ALPHA WIDGETS
En esta página encontrarás una herramienta que te convierte estructuras esqueletales en estructuras de Lewis
Muy buena
CHEMDOODLE WEB COMPONENTS
LEWIS DOT STRUCTURES
EXCEPCIONES A LA REGLA DEL OCTETO
ESPECIES CON UN NÚMERO IMPAR DE ELECTRONES


ESPECIES CON ÁTOMOS DE BERILIO O BORO (segundo periodo del sistema periódico), QUE FORMAN OCTETOS INCOMPLETOS


ESPECIES CON ÁTOMOS DE AZUFRE, FÓSFORO O CLORO (tercer periodo del sistema periódico), QUE FORMAN OCTETOS EXPANDIDOS


ESPECIES EN LAS QUE EL CUMPLIMIENTO DE LA REGLA DEL OCTETO IMPLICARÍA UN EXCESO DE CARGAS FORMALES

Si el átomo de azufre cumpliera la regla del octeto en el ion sulfato, habría un exceso de cargas formales, los cinco átomos que forman el ion tendrían cargas formales. Sin embargo, sólo son estables las especies químicas que tienen una o dos cargas formales, por tanto, es necesario aceptar que el átomo de azufre forma dos enlaces dobles, rodeándose de 12 electrones e incumpliendo la regla del octeto. De esa manera en el ion sulfato sólo hay dos átomos que tienen cargas formales.
GEOMETRÍA MOLECULAR
MÉTODO DE REPULSIÓN DE PARES DE ELECTRONES DE LA CAPA DE VALENCIA (MRPECV)
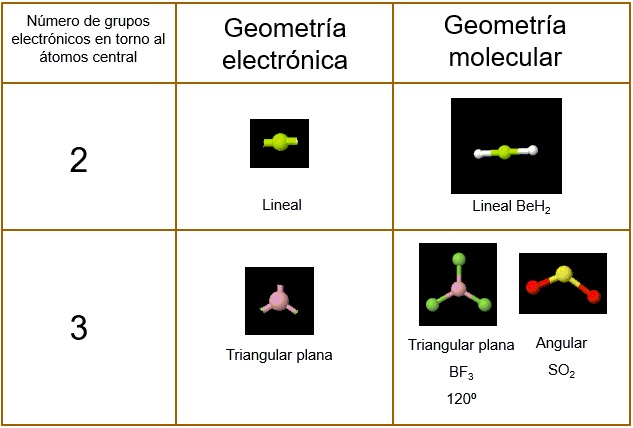
Las estructuras de Lewis no indican la geometría de las especies químicas pero permiten determinarla si a ellas se les aplica el MRPECV:
Los pares de electrones se disponen en torno al átomo central de la molécula de modo que se minimicen las repulsiones eléctricas entre ellos, es decir lo más alejados posible
REGLAS PARA APLICAR EL MRPECV
- Dibuje la estructura de Lewis de la especie química
-Cuente el número de regiones de alta densidad electrónica (enlaces o pares de electrones solitarios) en torno al átomo central
-Identifique la forma más estable de colocar esas regiones de alta densidad electrónica (GEOMETRÍA ELECTRÓNICA)
-Coloque los átomos exteriores en torno al átomo central respetando la disposición anterior (GEOMETRÍA MOLECULAR)
EJEMPLO: Amoniaco
1.- Construir la estructura de Lewis
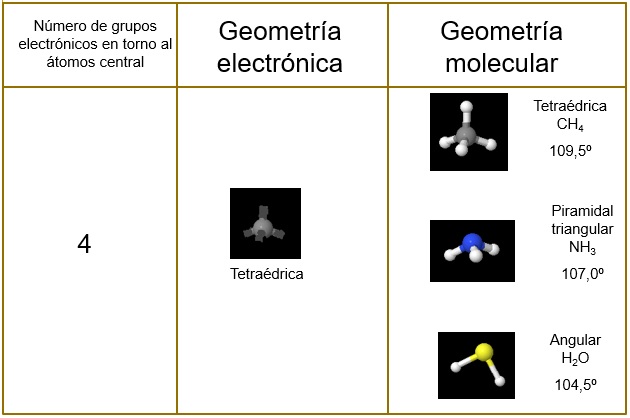
El amoniaco tiene 4 grupos electrónicos en torno al átomo central de la molécula (tres enlaces y un par no compartido)
2.- Determinar la geometría electrónica de la molécula:
Tetraédrica: Los 4 grupos electrónicos se colocan lo más separados posible, es decir, se orientan hacia los vértices de un tetraedro.
3.- Determinar la geometría molecular:
Piramidal: De los cuatro grupos que rodean el átomo de nitrógeno, solo tres de ellos se unen a átomos de hidrógeno. Por tanto, la molécula de amoniaco tiene forma piramidal triangular.
FORMA DE MOLÉCULAS CON PHET
CHEMDOODLE WEB COMPONENTS
2 TO 3D COORDINATES
En esta página encontrarás una herramienta que te convierte la estructura esqueletal en una estructura 3D
Con ella podrás comprobar ángulos y formas que en el plano son difíciles de visualizar





